La malattia

La demenza č una sindrome clinica (insieme di sintomi) dovuta ad una malattia cronica che colpisce il cervello e lentamente porta la persona alla morte.
In particolare deteriorano piano piano le facoltŕ mentali come la memoria, il linguaggio, l'orientamento spazio-temporale e la capacitŕ di ragionamento. Col progressivo peggioramento di queste abilitŕ la persona presenta difficoltŕ sempre maggiori nel riconoscere oggetti e persone, lavorare, curare l'igiene della propria persona e della casa, preparare i pasti, ecc.
Sin dall'inizio, ed in maniera assai variabile da caso a caso, insorgono problemi di umore come depressione, ansia ed angoscia.
A seconda della causa della demenza, inoltre, possono comparire disturbi del comportamento come agitazione, aggressivitŕ, reazioni paranoiche ed apatia.
Durata di malattia:
la diagnosi di demenza in genere viene fatta dal medico mediamente dopo 18-36 mesi dalla comparsa dei primi sintomi. La durata della malattia varia dai 3 ai 18 anni: č dimostrato che sulla durata di malattia influiscono negativamente altre malattie concomitanti e l'uso di farmaci neurolettici.
Forme cliniche di demenza ( ):
-
malattia di Alzheimer, 50 – 65%
-
demenza vascolare: 11 – 24%
-
demenza a corpi di Lewy: 10 – 15%
-
demenza fronto-temporale ed altre forme di demenza: 4%
Quanti sono gli ammalati ?
Si dice che gli ammalati in Italia siano almeno 500.000 (c'č chi dice che sono 800.000).
La malattia colpisce il 6,4% (studio ILSA, Italia, 1997) delle persone ultrasessantacinquenni. La percentuale aumenta considerando fasce di popolazione piů anziane: sopra i 90 anni la percentuale supera il 40 %.
Qualche elemento di speranza.
In un recente articolo scientifico Schrijvers (Neurology, 2012.) ha confrontato l'incidenza della demenza nella cittŕ di Rotterdam nel 1990 e nel 2000: considerando tutte le fasce d'etŕ nel 2000 la demenza non č aumentata, anzi č calata del 15%.
Nello studio del Karolinska Institute di Stoccolma (Fratiglioni, 2009) č stata seguito un grande numero di anziani della Svezia dal 1987. Ebbene, č stato dimostrato che esistono fattori protettivi verso la demenza come 1) mantenere una estesa rete di contatti sociali 2) fare attivitŕ fisica, 3) svolgere attivitŕ di impegno mentale.

Il morbo di Alzheimer č una forma di demenza irreversibile e progressiva che distrugge lentamente la memoria e le capacitŕ cognitive e, infine, impedisce al paziente di portare a termine persino i compiti piů semplici. Nella maggior parte delle persone affette dal morbo di Alzheimer i sintomi compaiono per la prima volta dopo i 60 anni.
Il morbo di Alzheimer č la forma di demenza senile piů comune, demenza significa perdita delle capacitŕ cognitive (pensiero, memoria e ragionamento) in misura tale da interferire con la vita e le attivitŕ quotidiane della persona: secondo stime recenti in Italia i malati di Alzheimer sono circa 520.000 ed i nuovi casi sono stimabili in circa 80.000 all’anno.
La malattia deve il suo nome allo scopritore, un medico che si chiamava Alois Alzheimer, che nel 1906 scoprě dei cambiamenti nel tessuto cerebrale di una donna deceduta per una strana malattia mentale. Tra i suoi sintomi c’erano perdite di memoria, problemi di linguaggio e imprevedibilitŕ del comportamento. A seguito della morte il medico esaminň il suo cervello e scoprě molte macchie anomale (che ora vengono definite placche amiloidi) e grovigli di fibre (ora definiti ammassi neurofibrillari).
Le placche e gli ammassi all’interno del cervello sono due delle caratteristiche biologiche del morbo di Alzheimer, la terza caratteristica č la perdita di connessioni tra le cellule nervose (i neuroni) del cervello.

Essa č stata descritta per la prima volta nel 1906, dallo psichiatra e neuropatologo tedesco Alois Alzheimer. Nel 2006 vi erano 26,6 milioni malati di tutto il mondo, e si stima che ne sarŕ affetta 1 persona su 85 a livello mondiale entro il 2050.
La sua ampia e crescente diffusione nella popolazione, la limitata e comunque non risolutiva efficacia delle terapie disponibili, e le enormi risorse necessarie per la sua gestione (sociali, emotive, organizzative ed economiche), che ricadono in gran parte sui familiari dei malati, la rendono una delle patologie a piů grave impatto sociale del mondo.
Anche se il decorso clinico della malattia di Alzheimer č in parte specifico per ogni individuo, la patologia causa diversi sintomi comuni alla maggior parte dei pazienti. I primi sintomi osservabili sono spesso erroneamente considerati problematiche "legate all'etŕ", o manifestazioni di stress. Nelle prime fasi, il sintomo piů comune č l'incapacitŕ di acquisire nuovi ricordi e la difficoltŕ nel ricordare eventi osservati recentemente. Quando si ipotizza la presenza di un possibile morbo di Alzheimer, la diagnosi viene di solito confermata tramite specifiche valutazioni comportamentali e test cognitivi, spesso seguiti dall'imaging a risonanza magnetica.
Con l'avanzare della malattia, il quadro clinico puň prevedere confusione, irritabilitŕ e aggressivitŕ, sbalzi di umore, difficoltŕ nel linguaggio, perdita della memoria a lungo termine e progressive disfunzioni sensoriali.
La causa e la progressione della malattia di Alzheimer non sono ancora ben compresi. La ricerca indica che la malattia č associata a placche amiloidi e ammassi neurofibrillari nel cervello. Attualmente i trattamenti terapeutici utilizzati offrono piccoli benefici sintomatici, e possono parzialmente rallentare il decorso della patologia; anche se sono stati condotti oltre 500 studi clinici per l'identificazione di un possibile trattamento per l'Alzheimer, non sono ancora stati identificati trattamenti che ne arrestino o invertano il decorso. A livello preventivo, sono state proposte diverse modificazioni degli stili di vita personali come potenziali fattori protettivi nei confronti della patologia, ma non vi sono adeguate prove di una correlazione certa tra queste raccomandazioni e la riduzione effettiva della degenerazione. Stimolazione mentale, esercizio fisico e una dieta equilibrata sono state proposte sia come modalitŕ di possibile prevenzione, che come modalitŕ complementari di gestione della malattia.
Poiché per il morbo di Alzheimer non sono attualmente disponibili terapie risolutive ed il suo decorso č progressivo, la gestione dei bisogni dei pazienti diviene essenziale. Spesso č il coniuge o un parente stretto a prendersi in carico il malato (caregiver), compito che comporta notevoli difficoltŕ e oneri. Chi si occupa del paziente puň sperimentare pesanti carichi personali, che possono coinvolgere aspetti sociali, psicologici, fisici ed economici.

Non si conoscono con esattezza quali siano le cause del morbo di Alzheimer, ma sappiamo che i danni al cervello iniziano a comparire giŕ 10 o 20 anni prima che i sintomi diventino evidenti nel comportamento.
Gli ammassi iniziano a svilupparsi in una zona profonda del cervello (la corteccia entorinale), mentre le placche si formano in altre zone. Con la formazione delle placche e degli ammassi i neuroni sani iniziano a perdere efficienza, in seguito cominciano a non funzionare piů e a non comunicare piů tra di loro ed alla fine muoiono.
Questo processo di degrado si diffonde in una struttura vicina, l’ippocampo, che č necessaria per il processo di memorizzazione. Piů i neuroni muoiono, piů le zone del cervello colpite iniziano a rimpicciolirsi. Con lo stadio finale del morbo di Alzheimer il danno č diffuso ovunque e il tessuto cerebrale si č ridotto in maniera significativa.
La malattia si sviluppa a causa di una complessa catena di eventi che avvengono nel cervello sul lungo periodo, probabilmente le cause sono legate a fattori di ordine genetico, ambientale e riguardanti lo stile di vita. Poiché le informazioni genetiche e lo stile di vita delle persone variano molto, l’importanza di questi fattori per prevenire il morbo di Alzheimer, oppure per rallentarne il decorso, varia da persona a persona.
I fondamenti.
I ricercatori stanno compiendo ricerche per conoscere meglio le placche, gli ammassi e le altre caratteristiche del morbo di Alzheimer. Ora hanno la possibilitŕ di vedere le placche tramite l’imaging del cervello di persone vive. Stanno anche esplorando le primissime fasi della malattia. Le scoperte fatte grazie a queste ricerche li aiuteranno a comprendere le cause del morbo di Alzheimer.
Uno dei misteri legati al morbo di Alzheimer č perché colpisca quasi esclusivamente gli anziani, per far luce su questo fatto sono in corso ricerche sulle modalitŕ normali di invecchiamento del cervello: ad esempio i ricercatori stanno scoprendo in che modo le alterazioni del cervello dovute all’invecchiamento possano danneggiare i neuroni e contribuire cosě alla comparsa del morbo. Tra questi cambiamenti legati all’invecchiamento troviamo l’infiammazione e la produzione di molecole instabili, i cosiddetti radicali liberi.
Fattori genetici.
In rari casi i pazienti sviluppano il morbo di Alzheimer tra i 30 e i 50 anni perchč per loro la malattia č ereditaria: in queste persone si ha una mutazione, ovvero un cambiamento definitivo, in uno dei geni ereditati da un genitore. Sappiamo che queste mutazioni genetiche causano il morbo di Alzheimer con esordio precoce.
Al contrario, nella maggior parte della popolazione colpita, l’esordio dell’Alzheimer č tardivo e di solito avviene dopo i 60 anni.
Fattori legati allo stile di vita.
Una dieta completa, il regolare esercizio fisico, una sana vita sociale e occupazioni che stimolino la mente possono aiutare a rimanere in salute. Le nuove ricerche suggeriscono la possibilitŕ che questi fattori potrebbero essere utili per diminuire il rischio di deficit cognitivi e Alzheimer, gli scienziati stanno compiendo ricerche sulla connessione tra i problemi cognitivi dovuti all’invecchiamento e le malattie cardiache, l’ipertensione, il diabete e l’obesitŕ. Capire queste connessioni e rilevarle con gli esperimenti clinici ci aiuterŕ a comprendere se riducendo i fattori di rischio per queste altre malattie avrŕ una qualche utilitŕ anche per combattere il morbo di Alzheimer.

Epidemiologia
|
ETA' |
Nuovi casi per migliaia di persone all'anno |
|
65-69 |
3 |
|
70-74 |
6 |
|
75-79 |
9 |
|
80-84 |
23 |
|
85-89 |
40 |
|
90-> |
69 |
La malattia (o morbo) di Alzheimer č definibile come un processo degenerativo che pregiudica progressivamente le cellule cerebrali, rendendo a poco a poco l'individuo che ne č affetto incapace di una vita normale e provocandone alla fine la morte. In Italia ne soffrono circa 800.000 persone, e 26.6 milioni nel mondo secondo uno studio della Johns Hopkins Bloomberg School of Public Health di Baltimora, USA, con una netta prevalenza di donne (per via della maggior vita media delle donne rispetto agli uomini).
Definita anche "demenza di Alzheimer", viene appunto catalogata tra le demenze, essendo un deterioramento cognitivo cronico progressivo. Tra tutte le demenze quella di Alzheimer č la piů comune, rappresentando, a seconda della casistica, l'80-85% di tutti i casi di demenza.
A livello epidemiologico, tranne che in rare forme genetiche famigliari "early-onset" (cioč ad esordio giovanile), il fattore maggiormente correlato all'incidenza della patologia č l'etŕ. Molto rara sotto i 65 anni, la sua incidenza aumenta progressivamente con l'aumentare dell'etŕ, per raggiungere una diffusione significativa nella popolazione oltre gli 85 anni.
Da rilevazioni europee, nella popolazione generale l'incidenza (cioč il numero di nuovi casi all'anno) č di 2,5 casi ogni 1.000 persone per la fascia di etŕ tra i 65 ed i 69 anni; sale a 9 casi su 1.000 persone tra i 75 ed i 79 anni, ed a 40,2 casi su 1.000 persone tra gli 85 e gli 89 anni.
Costi economico-sociali.
La crescente incidenza di questa patologia nella popolazione generale in tutto il mondo č accompagnata da una crescita equivalente del suo enorme costo economico e sociale: allo stato, secondo Lancet, il costo economico per la cura dei pazienti affetti da demenza a livello mondiale č di circa 600 miliardi di dollari all'anno, con un trend di crescita che lo porterŕ nel 2030 ad aumentare dell'85% (e con un carico crescente anche per i Paesi in via di sviluppo), facendolo divenire uno degli oneri con maggior impatto economico per i sistemi sanitari nazionali e le comunitŕ sociali dell'intero pianeta.
Nonostante questo, la ricerca scientifica e clinica sulla demenza č ancora gravemente sottofinanziata: in Inghilterra, ad esempio, si calcola che il costo economico complessivo della cura dei pazienti affetti da demenza superi quello per i tumori e per le malattie cardiovascolari messe insieme, ma la ricerca sulle demenze riceve solo un dodicesimo dei finanziamenti di quella per i tumori.

Nel 1901, il dottor Alois Alzheimer, uno psichiatra tedesco, intervistň una sua paziente, la signora Auguste D., di 51 anni. Le mostrň parecchi oggetti e successivamente le chiese che cosa le era stato indicato. Lei non poteva perň ricordare. Inizialmente registrň il suo comportamento come "disordine da amnesia di scrittura", ma la signora Auguste D. fu la prima paziente a cui venne diagnosticata quella che in seguito sarebbe stata conosciuta come malattia di Alzheimer. Negli anni successivi vennero registrati in letteratura scientifica undici altri casi simili; nel 1910 la patologia venne inserita per la prima volta dal grande psichiatra tedesco Emil Kraepelin nel suo classico Manuale di Psichiatria, venendo da lui definita come "Malattia di Alzheimer", o "Demenza Presenile". Il termine, inizialmente utilizzato solo per le rare forme "early-onset" (ovvero, con esordio clinico prima dei 65 anni), dopo il 1977 č stato ufficialmente esteso a tutte le forme di Alzheimer.

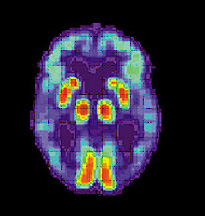
Immagine PET del cervello di una persona con morbo di Alzheimer che mostra la perdita di funzione del lobo temporale.
Il decorso della malattia puň essere diverso, nei tempi e nelle modalitŕ sintomatologiche, per ogni singolo paziente; esistono comunque una serie di sintomi comuni, che si trovano frequentemente associati nelle varie fasi con cui, clinicamente, si suddivide per convenzione il decorso della malattia. Ad una prima fase lieve, fa seguito la fase intermedia, e quindi la fase avanzata/severa; il tempo di permanenza in ciascuna di queste fasi č variabile da soggetto a soggetto, e puň in certi casi durare anche diversi anni.
La malattia viene spesso anticipata dal cosiddetto mild cognitive impairment (MCI), un leggero calo di prestazioni in diverse funzioni cognitive in particolare legate alla memoria, all'orientamento o alle capacitŕ verbali. Tale calo cognitivo, che č comunque frequente nella popolazione anziana, non č necessariamente indicativo di demenza incipiente, puň in alcuni casi essere seguito dall'avvio delle fasi iniziali dell'Alzheimer.
La malattia si manifesta spesso inizialmente come demenza caratterizzata da amnesia progressiva ed altri deficit cognitivi. Il deficit di memoria č prima circoscritto a sporadici episodi nella vita quotidiana, ovvero disturbi di quella che viene chiamata on-going memory (ricordarsi cosa si č mangiato a pranzo, cosa si č fatto durante il giorno) e della memoria prospettica (che riguarda l'organizzazione del futuro prossimo, come ricordarsi di andare a un appuntamento); poi man mano il deficit aumenta e la perdita della memoria arriva a colpire anche la memoria episodica retrograda (riguardante fatti della propria vita o eventi pubblici del passato) e la memoria semantica (le conoscenze acquisite), mentre la memoria procedurale (che riguarda l'esecuzione automatica di azioni) viene relativamente risparmiata fino alle fasi intermedio-avanzate della malattia.
A partire dalle fasi lievi e intermedie possono poi manifestarsi crescenti difficoltŕ di produzione del linguaggio, con incapacitŕ nella definizione di nomi di persone od oggetti, e frustranti tentativi di "trovare le parole", seguiti poi nelle fasi piů avanzate da disorganizzazione nella produzione di frasi ed uso sovente scorretto del linguaggio (confusione sui significati delle parole, etc.). Sempre nelle fasi lievi-intermedie, la pianificazione e gestione di compiti complessi (gestione di documenti, attivitŕ lavorative di concetto, gestione del denaro, guida dell'automobile, cucinare, etc.) iniziano a diventare progressivamente piů impegnative e difficili, fino a richiedere assistenza continuativa o divenire impossibili.
Nelle fasi intermedie ed avanzate, inoltre, possono manifestarsi problematiche comportamentali (vagabondaggio, coazione a ripetere movimenti o azioni, reazioni comportamentali incoerenti) o psichiatriche (confusione, ansia, depressione, ed occasionalmente deliri e allucinazioni). Il disorientamento nello spazio, nel tempo o nella persona (ovvero la mancata o confusa consapevolezza di dove si č situati nel tempo, nei luoghi e/o nelle identitŕ personali, proprie o di altri – comprese le difficoltŕ di riconoscimento degli altri significativi) č sintomo frequente a partire dalle fasi intermedie-avanzate. In tali fasi si aggiungono difficoltŕ progressive anche nella cura della persona (lavarsi, vestirsi, assumere farmaci, etc.).
Ai deficit cognitivi e comportamentali, nelle fasi piů avanzate si aggiungono infine complicanze mediche internistiche, che portano a una compromissione progressiva della salute. Una persona colpita dal morbo puň vivere anche una decina di anni dopo la diagnosi clinica di malattia conclamata.
Come sottolineato, col progredire della malattia le persone non solo presentano deficit di memoria, ma risultano deficitarie nelle funzioni strumentali mediate dalla corteccia associativa, e possono pertanto presentare afasia e aprassia, fino a presentare disturbi neurologici e poi internistici; pertanto i pazienti, nelle fasi intermedie ed avanzate, necessitano di continua assistenza personale (solitamente erogata da famigliari e badanti, i cosiddetti caregivers, che sono a loro volta sottoposti ai forti stress tipici di chi assiste i malati di Alzheimer).

Il morbo di Alzheimer č una malattia complessa e non esiste alcuna bacchetta magica in grado di prevenirlo o di curarlo. Questo č il motivo per cui le terapie che oggi abbiamo a disposizione si concentrano su diversi aspetti, tra cui:
-
la salvaguardia delle capacitŕ mentali,
-
la gestione dei sintomi comportamentali
-
il rallentamento del decorso della malattia,
-
la prevenzione.
Salvaguardia delle capacitŕ mentali
Esistono quattro farmaci approvati dalla Food and Drug Administration americana per la cura del morbo di Alzheimer:
-
donepezil (Aricept®),
-
rivastigmina (Exelon®)
-
galantamina (Reminyl®)
Questi 3 farmaci vengono usati per curare l’Alzheimer da lieve a moderato (il donepezil puň anche essere usato per l’Alzheimer grave).
-
nemantina (Namenda®)
Quest’ultima viene usata per curare l’Alzheimer da moderato a grave, ma al momento non č in commercio in Italia.
Il funzionamento di questi farmaci si basa sulla regolazione dei neurotrasmettitori (le sostanze chimiche che trasmettono i messaggi tra i neuroni), possono contribuire alla salvaguardia del pensiero, della memoria e delle abilitŕ di parola e dimostrarsi efficaci con determinati problemi comportamentali. Tuttavia questi farmaci non modificano il decorso della malattia e possono dimostrarsi utili solo per un periodo che va da alcuni mesi ad alcuni anni.
Gestione dei sintomi comportamentali
Tra i sintomi comportamentali piů comuni del morbo di Alzheimer troviamo:
-
insonnia,
-
agitazione,
-
vagabondaggio,
-
ansia,
-
aggressivitŕ,
-
depressione.
I ricercatori stanno scoprendo perché si verificano questi sintomi e stanno studiando nuove terapie, farmacologiche e non, per gestirli. La terapia dei sintomi comportamentali spesso rende piů autonomi i malati di Alzheimer e facilita il compito di chi li assiste.

Anche se al momento non esiste una cura efficace, sono state proposte diverse strategie terapeutiche per tentare di influenzare clinicamente il decorso del morbo di Alzheimer; tali strategie puntano a modulare farmacologicamente alcuni dei meccanismi patologici che ne stanno alla base. Č inoltre opportuno integrare interventi psicosociali, cognitivi e comportamentali, che hanno dimostrato effetti positivi, sinergicamente all'uso dei presidi farmacologici, nel rallentamento dell'evoluzione dei sintomi e nella qualitŕ della vita dei pazienti e dei caregivers.
Intervento farmacologico
In primo luogo, basandosi sul fatto che nell'Alzheimer si ha diminuzione dei livelli di acetilcolina, un'ipotesi terapeutica č stata quella di provare a ripristinarne i livelli fisiologici. L'acetilcolina pura non puň perň essere usata, in quanto troppo instabile e con un effetto limitato. Gli agonisti colinergici invece avrebbero effetti sistemici e produrrebbero troppi effetti collaterali, e non sono quindi utilizzabili. Si possono invece usare gli inibitori della colinesterasi, l'enzima che catabolizza l'acetilcolina: inibendo tale enzima, si aumenta la quantitŕ di acetilcolina presente nello spazio intersinaptico.
Sono a disposizione farmaci inibitori dell'acetilcolinesterasi, che hanno una bassa affinitŕ per l'enzima presente in periferia, e che sono sufficientemente lipofili da superare la barriera emato-encefalica (BEE), e agire quindi di preferenza sul sistema nervoso centrale. Tra questi la tacrina, il donepezil, la fisostigmina, la galantamina e la neostigmina sono stati i capostipiti, ma l'interesse farmacologico č attualmente maggiormente concentrato sugli inibitori reversibili della acetilcolinesterasi, quali la rivastigmina e lagalantamina stessa.
Un'altra, piů recente, linea d'azione prevede il ricorso a farmaci che agiscano direttamente sul sistemaglutamatergico, come la memantina. La memantina ha dimostrato un'attivitŕ terapeutica, moderata ma positiva, nella parziale riduzione del deterioramento cognitivo in pazienti con Alzheimer da moderato a grave.
La tacrina non č piů utilizzata perché epatotossica, mentre il donepezil, inibitore non competitivo dell'acetilcolinesterasi, sembrerebbe piů efficace perché, con una emivita di circa 70 ore, permette una sola somministrazione al giorno (mentre la galantamina ha una emivita di 7 ore). Ovviamente perň il donepezil č piů soggetto a manifestare effetti collaterali dovuti ad un aumento del tono colinergico (quali insonnia, aritmie, bradicardia, nausea, diarrea). Di contro, la galantamina e la rivastigmina possono causare gli stessi effetti, ma in misura molto minore.
Altre ipotesi di approccio farmacoterapico
Oltre alle molecole e strategie di intervento giŕ delineate, sono state variamente proposte altre ipotesi di intervento farmacologico, con evidenze cliniche di efficacia perň insufficienti o non confermate.
Tra esse, un'altra ipotesi complementare di approccio alla patologia č legata alla proposta d'uso di FANS (anti-infiammatori non steroidei). Come detto, nell'Alzheimer č presente una dinamica infiammatoria che danneggia i neuroni. L'uso di antiinfiammatori č stato quindi ipotizzato che potrebbe migliorare la condizione clinica dei pazienti. Si č anche notato che le donne in cura post-menopausale con farmaci estrogeni presentano una minor incidenza della patologia (infatti gli estrogeni bloccano la morte neuronale indotta dalla proteina beta-amiloide) Alcuni ricercatori avrebbero messo in evidenza anche la potenziale azione protettiva della vitamina E (alfa-tocoferolo), che sembrerebbe prevenire la perossidazione lipidica delle membrane neuronali causata dal processo infiammatorio; ma ricerche piů recenti non hanno confermato l'utilitŕ della vitamina E (né della vitamina C) nella prevenzione primaria e secondaria della patologia, sottolineando anzi i potenziali rischi sanitari legati all'eccessiva e prolungata assunzione di vitamina E.
Sul processo neurodegenerativo puň intervenire anche l'eccitotossicitŕ, ossia un'eccessiva liberazione di acidiGlutammico ed Aspartico, entrambi neurotrasmettitori eccitatori, che inducono un aumento del calcio libero intracellulare, il quale č citotossico. Si č quindi ipotizzato di usare farmaci antagonisti del glutammato e dell'aspartato, ma anche questi ultimi presentano notevoli effetti collaterali.
Sono presenti in commercio farmaci definiti Nootropi ("stimolanti del pensiero"), come il Piracetam e l'Aniracetam: questi farmaci aumentano il rilascio di Acido glutammico; anche se questo parrebbe in netta contrapposizione a quanto detto sopra, si deve tenere presente che comunque tale neurotrasmettitore č direttamente implicato nei processi di memorizzazione e di apprendimento. Aumentandone la quantitŕ, č stato ipotizzato di poter contribuire a migliorare i processi cognitivi. Anche in questo caso, l'evidenza clinica di efficacia č scarsa.
Ultimo approccio ipotizzato č l'uso di Pentossifillina e Diidroergotossina (sembra che tali farmaci migliorino il flusso ematico cerebrale, permettendo cosě una migliore ossigenazione cerebrale, ed un conseguente miglioramento delle performance neuronali). Sempre per lo stesso scopo č stato proposto l'uso del Gingko biloba, ma l'evidenza scientifica a supporto di questa tesi č negativa.
Intervento psicosociale e cognitivo

Una stanza speciale progettata per la terapia di riabilitazione sensoriale.
Le forme di trattamento non-farmacologico consistono prevalentemente in interventi comportamentali, di supporto psicosociale e di training cognitivo. Tali misure sono solitamente integrate in maniera complementare con il trattamento farmacologico, ed hanno dimostrato una loro efficacia positiva nella gestione clinica complessiva del paziente.
I training cognitivi (di diverse tipologie, e con diversi obbiettivi funzionali: Reality-Orientation Therapy,Validation Therapy, Reminescence Therapy, i vari programmi di stimolazione cognitiva – Cognitive Stimulation Therapy, etc.), hanno dimostrato risultati positivi sia nella stimolazione e rinforzo delle capacitŕ neurocognitive, che nel miglioramento dell'esecuzione dei compiti di vita quotidiana. I diversi tipi di intervento si possono rivolgere prevalentemente alla sfera cognitiva (ad es., Cognitive Stimulation Therapy), comportamentale (Gentlecare, programmi di attivitŕ motoria), sociale ed emotivo-motivazionale (ad es., Reminescence Therapy,Validation Therapy, etc.).
La Reality-Orientation Therapy, focalizzata su attivitŕ formali ed informali di orientamento spaziale, temporale e sull'identitŕ personale, ha dimostrato in diversi studi clinici di poter facilitare la riduzione del disorientamento soggettivo, e contribuire a rallentare il declino cognitivo, soprattutto se effettuata con regolaritŕ nelle fasi iniziali e intermedie della patologia.
I vari programmi di stimolazione cognitiva (Cognitive Stimulation), sia eseguiti a livello individuale (eseguibili anche presso il domicilio dai caregivers, opportunamente formati), che in sessioni di gruppo, possono rivestire una significativa utilitŕ nel rallentamento dei sintomi cognitivi della malattia, e, a livello di economia sanitaria, presentano un ottimo rapporto tra costi e benefici. La stimolazione cognitiva, oltre a rinforzare direttamente le competenze cognitive di tipo mnestico, attentivo e di pianificazione, facilita anche lo sviluppo di "strategie di compensazione" per i processi cognitivi lesi, e sostiene indirettamente la "riserva cognitiva" dell'individuo.
La Reminescence Therapy (fondata sul recupero e la socializzazione di ricordi di vita personale positivi, con l'assistenza di personale qualificato e materiali audiovisivi), ha dimostrato risultati interessanti sul miglioramento dell'umore, dell'autostima e delle competenze cognitive, anche se ulteriori ricerche sono ritenute necessarie per una sua completa validazione.
Forme specifiche di musicoterapia ed arteterapia, attuate da personale qualificato, possono essere utilizzate per sostenere il tono dell'umore e forme di socializzazione nelle fasi intermedio-avanzate della patologia, basandosi su canali di comunicazione non verbali.
Positivo sembra essere anche l'effetto di una moderata attivitŕ fisica e motoria, soprattutto nelle fasi intermedie della malattia, sul tono dell'umore, sul benessere fisico e sulla regolarizzazione dei disturbi comportamentali, del sonno e alimentari.
Fondamentale č inoltre la preparazione ed il supporto, informativo e psicologico, rivolto ai "caregivers" (parenti e personale assistenziale) del paziente, che sono sottoposti a stress fisici ed emotivi significativi, in particolare con l'evoluzione della malattia.
Una chiara informazione ai famigliari, una buona alleanza di lavoro con il personale sanitario, e la partecipazione a forme di supporto psicologico diretto (spesso tramite specifici gruppi di auto-mutuo-aiuto tra pari), oltre all'eventuale coinvolgimento in associazioni di famigliari, rappresentano essenziali forme di sostegno per l'attivitŕ di cura.
Sempre nello stesso senso appare di particolare utilitŕ, solitamente a partire dalle fasi intermedie della patologia, l'inserimento del paziente per alcune ore al giorno nei Centri Diurni, presenti in molte cittŕ (attivitŕ che puň portare benefici sia per la stimolazione cognitiva e sociale diretta del paziente, che per il supporto sociale indiretto ai caregivers).
La cura dell'Alzheimer č perň ai primi passi: al momento non esistono ancora farmaci o interventi psicosociali che guariscano o blocchino la malattia. Si puň migliorare la qualitŕ della vita dei pazienti malati, e provare a rallentarne il decorso nelle fasi iniziali e intermedie.

Assistere un malato di Alzheimer puň avere enormi costi fisici, emotivi e finanziari. Le necessitŕ di cura quotidiana, il cambiamento dei ruoli all’interno della famiglia e la difficoltŕ di decidere verso quale struttura indirizzare il malato possono essere difficili da affrontare.
Una strategia importante, valida sul lungo periodo, č quella di documentarsi il piů possibile sull’Alzheimer: i programmi che insegnano alle famiglie quali sono le varie fasi dell’Alzheimer e quali strategie e pratiche flessibili adottare quando la cura del malato č piů difficile, forniscono un aiuto di vitale importanza a tutti coloro che assistono un paziente.
Anche sviluppare le opportune strategie di convivenza con la malattia e una forte rete di aiuto, costituita da famigliari e amici, sono due modi importanti con cui chi assiste il malato puň gestire lo stress dovuto all’assistenza continua: ad esempio, se si fa attivitŕ fisica si possono avere ricadute positive sul fisico e sull’umore.
Alcune persone che assistono ritengono che partecipare a un gruppo di aiuto apposito sia una vera e propria ancora di salvezza, questi gruppi permettono a chi assiste un malato di trovare un momento di tregua, di esprimere le proprie preoccupazioni, di condividere il proprio vissuto, di ricevere consigli e solidarietŕ emotiva.

La diagnosi di Alzheimer diventa definitiva solo dopo la morte del paziente ed il decorso della malattia viene messo in relazione con gli esiti dell’esame autoptico del tessuto cerebrale.
Al giorno d’oggi i medici hanno diversi metodi e strumenti per determinare con sufficiente accuratezza se una persona con problemi di memoria č affetta da Alzheimer possibile (quando i sintomi potrebbero anche essere dovuti a un’altra causa) oppure probabile (quando non si riesce a individuare nessun’altra causa per i sintomi).
Per diagnosticare il morbo di Alzheimer, i medici:
-
si informano sullo stato di salute generale del paziente, sui problemi clinici avuti in passato, sulla capacitŕ di svolgere le attivitŕ quotidiane e sugli eventuali cambiamenti del comportamento e della personalitŕ.
-
somministrano test riguardanti la memoria, la capacitŕ di risolvere problemi, l’attenzione, la capacitŕ di contare e il linguaggio
-
consigliano altri esami clinici, ad esempio esami del sangue, delle urine o del midollo spinale
-
esaminano il cervello, con esami come la tomografia computerizzata (TC) o la risonanza magnetica.
Questi esami possono essere ripetuti per dare informazioni su come la memoria del paziente varia nel corso del tempo.
La diagnosi precoce č utile per diversi motivi. Se la malattia viene diagnosticata precocemente e si inizia la terapia quando č ancora nei primi stadi si puň conservare la funzionalitŕ del cervello per mesi o addirittura anni, anche se il processo degenerativo dovuto all’Alzheimer non puň essere arrestato. La diagnosi precoce puň anche aiutare le famiglie a fare progetti per il futuro, a trovare una casa piů adatta al malato, a occuparsi delle questioni finanziarie e legali e a sviluppare reti di supporto.
Diagnosi clinica
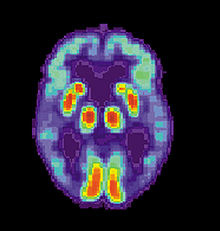
Immagine PET del cervello di una persona con morbo di Alzheimer che mostra la perdita di funzione del lobo temporale.
La malattia di Alzheimer č di solito diagnosticata clinicamente dalla storia del paziente, da osservazioni cliniche, dalla presenza di peculiari caratteristiche neurologiche e neuropsicologiche e per l'assenza di condizioni alternative.
Sistemi avanzati di imaging biomedico, come la tomografia computerizzata (TC), la risonanza magnetica (MRI), la tomografia a emissione di fotone singolo (SPECT) o la tomografia ad emissione di positroni (PET) possono essere utilizzate per aiutare ad escludere altre patologie cerebrali o altri tipi di demenza. Inoltre, si possono prevedere il passaggio da fasi prodromiche (decadimento cognitivo lieve) al morbo di Alzheimer.
Gli assessment neuropsicologici e cognitivi, inclusi i test di memoria ed esecutivi, possono ulteriormente caratterizzare lo stato della malattia. Diverse organizzazioni mediche hanno creato i criteri diagnostici per facilitare e standardizzare il processo diagnostico. La diagnosi clinica viene confermata a livello patologico solo con l'analisi istologica del cervello post-mortem.
Criteri diagnostici
Lo statunitense National Institute of Neurological Disorders and Stroke (NINCDS) e l'Associazione dei Malati di Alzheimer ha istituito il criterio diagnostico NINCDS-ADRDA nel 1984, in seguito aggiornato nel 2007. Questo criterio richiede che la presenza di deficit cognitivi e una sospetta sindrome di demenza debbano essere confermati da test neuropsicologici per porre la diagnosi clinica di Alzheimer. Una conferma istopatologica, tra cui un esame al microscopio del tessuto cerebrale (eseguibile solo post-mortem) č necessaria per una conferma della diagnosi definitiva a posteriori.
Sono otto gli ambiti funzionali cognitivi piů comunemente compromessi: memoria, linguaggio, abilitŕ percettiva, attenzione, abilitŕ costruttiva, orientamento, risoluzione dei problemi e capacitŕ funzionali. Questi ambiti cognitivi sono equivalenti ai criteri della NINCDS ADRDA, come elencati nel Diagnostic and Statistical Manual of Mental Disorders (DSM) pubblicato dalla American Psychiatric Association.
Tecniche diagnostiche
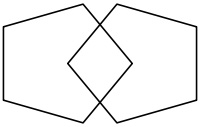
Alcuni test di screening neuropsicologico possono essere utili nella diagnosi di Alzheimer
Diversi test di screening neuropsicologico vengono utilizzati per la diagnostica nei casi di Alzheimer. I test valutano diverse funzioni e competenze cognitive, come il saper copiare disegni simili a quelli mostrati nella foto, ricordare parole, leggere e sottrarre numeri in serie.
Test neuropsicologici come il Mini Mental State Examination (MMSE), sono ampiamente utilizzati per valutare i disturbi cognitivi che vengono considerati per la formulazione della diagnosi. Una batteria di test piů completa č necessaria per garantire la massima affidabilitŕ dei risultati, in particolare nelle prime fasi della malattia. L'esame neurologico nelle prime fasi della malattia solitamente presenta risultati normali, fatta eccezione per evidenti deficit cognitivi che non differiscono perň da quello derivanti da altre malattie di tipo demenziale.
Ulteriori esami neurologici sono cruciali nella diagnosi differenziale di Alzheimer dalle altre malattie. Colloqui con gli altri membri della famiglia sono inoltre utilizzate nella valutazione funzionale della malattia. I caregiver possono infatti fornire importanti informazioni sulla capacitŕ di vita quotidiana, cosě come la diminuzione, nel tempo, della funzione mentale della persona.
Il punto di vista di chi assiste il malato č particolarmente importante, dato che una persona con Alzheimer č spesso inconsapevole del suo deficit.
A volte le famiglie hanno difficoltŕ nella rilevazione esatta dei primi sintomi di demenza nelle sue fasi iniziali, e per questo non riescono sempre a comunicare informazioni accurate al medico.
Un altro indicatore oggettivo delle prime fasi della malattia č l'analisi del liquido cerebrospinale per la ricerca di beta-amiloide o di proteine tau. La ricerca di queste proteine č in grado di prevedere l'insorgenza del morbo di Alzheimer con una sensibilitŕ compresa tra il 94% ed il 100%. Quando č utilizzata in combinazione con le tecniche di neuroimaging esistenti, i medici sono grado di identificare i pazienti che stanno giŕ sviluppando la malattia. Gli esami del liquido cerebrospinale sono disponibili piů facilmente, a differenza delle tecnologie di neuroimmaging piů moderne.Gli esami del liquido spinale sono disponibili piů facilmente, a differenza delle tecnologie di neuroimmaging piů moderne.
Altri test clinici supplementari forniscono informazioni aggiuntive su alcune caratteristiche della malattia, o venogono utilizzati per escludere altre diagnosi. E' comune eseguire test di funzionalitŕ tiroidea, valutare i livelli di vitamina B12, escludere la sifilide, escludere problemi metabolici (tra cui test per la funzione renale, i livelli di elettroliti e per il diabete), valutare i livelli di metalli pesanti (ad esempio il piombo e il mercurio), e l'anemia. E' anche necessario escludere la presenza di sintomatologia psichiatrica, quali deliri, disturbi dell'umore, disturbi del pensiero di natura psichiatrica, o pseudodemenze depressive.
In particolare vengono utilizzati test psicologici per la rilevazione della depressione, dal momento che la depressione puň essere concomitante con l'Alzheimer, essere un segno precoce di deficit cognitivo, o esserne addirittura la causa.
Imaging diagnostico
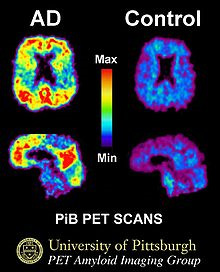
Questa immagine mostra una scansione PiB-PET di un paziente con malattia di Alzheimer a sinistra, e di una persona anziana con memoria normale sulla destra. Le aree di rosso e giallo mostrano alte concentrazioni di PiB, nel cervello che suggeriscono quantitŕ maggiori di depositi di Betamiloide
Se sono disponibili, la Tomografia a emissione di fotone singolo (SPECT) e la Tomografia a emissione di positroni (PET), possono essere utilizzati per la conferma di una diagnosi di Alzheimer in associazione con le valutazioni dello stato mentale. In una persona giŕ affetta da demenza, la SPECT sembra essere superiore nel differenziare la malattia di Alzheimer da altre possibili cause, rispetto all'analisi della storia famigliare e all'osservazione del paziente. I progressi hanno portato alla proposta di nuovi criteri diagnostici di imaging biomedico.
Una nuova tecnica nota come PiB PET č stata sviluppata per visualizzare direttamente e chiaramente immagini di depositi di beta-amiloide in vivo, utilizzando un radiotracciante che si lega selettivamente ai depositi A-beta.
La PiB-PET utilizza il carbonio-11 per la scansione PET. Studi recenti suggeriscono che la PiB-PET č precisa all'86% nel predire quali persone, giŕ affette da decadimento cognitivo lieve, svilupperanno la malattia di Alzheimer entro due anni, e al 92% in grado di escludere la probabilitŕ di sviluppare il morbo di Alzheimer.
Un radiofarmaco per PET chiamato (E)-4-(2-(6-(2-(2-(2-([18F]-fluoroethoxy)ethoxy)ethoxy)pyridin-3-yl)vinyl)-N-methyl benzenamine, o 18F AV-45, o florbetapir-fluorine-18, o semplicemente florbetapir, contenente il piů duraturo radionuclide fluoro-18, č stato recentemente realizzato e testato come possibile supporto diagnostico nella malattia di Alzheimer. Il florbetapir, come il PiB, si lega alla beta-amiloide, ma grazie all'uso del fluoro-18 ha una emivita di 110 minuti, in rapporto al tempo di dimezzamento radioattivo PiB che č di 20 minuti. La maggior durata permette di accumulare maggior tracciante nel cervello di persone con malattia di Alzheimer, in particolare nelle regioni note per essere associate a depositi di beta-amiloide.
La risonanza magnetica volumetrica č in grado di rilevare cambiamenti nella dimensione delle regioni del cervello. L'atrofia di queste regioni si sta mostrando come un indicatore diagnostico della malattia. Essa puň risultare meno costosa di altre tecniche di imaging attualmente in fase di studio.

La malattia si manifesta in forma insidiosa e progressiva, quindi non č sempre facile determinare quando č iniziata.
I primi sintomi sono disturbi della memoria e cambiamenti nel comportamento e nell'umore.
Top 10 dei segni del morbo di Alzheimer:
1. Perdita di memoria
Dimenticare appuntamenti, date, commissioni… sempre dei fatti recenti: "Chi č venuto a trovarmi ieri?", "Che cosa ho mangiato a pranzo?", "Chi ha chiamato al telefono?"
2. Frequente ripetizione delle stesse domande dopo ricevere le risposte
"Che ora č?", "Che ora č?" … oppure "Quando torna mia madre?", "Quando torna mia madre?"
3. Disposizione delle cose nei posti sbagliati
Si trovano le chiavi della macchina nella spazzatura, gli occhiali nascosti dentro una scarpa…oppure non ricordare dove ha messo le cose.
4. Difficoltŕ a ricordare i nomi degli oggetti comuni
"Dammi il … il …. Ah! Non mi ricordo come si chiama "
5. Perdita del senso di orientamento rispetto al posto e/o il tempo
"Che giorno č?" Quando č ovviamente una Domenica, "Dove mi trovo?" Quando č a casa. Perdersi sulla strada per la panetteria dove si acquista il pane ogni mattina.
6. Difficoltŕ nell’eseguire gesti semplici e comuni
Non riesce ad aprire la porta con la chiave, si commettono errori nel maneggiare la leva del cambio della macchina …
7. Perdita dell’interesse e della motivazione nello svolgere le attivitŕ che normalmente facevano con piacere.
Smettere di leggere il giornale, guardare i loro programmi TV preferiti, giocare a carte con gli amici…
8. Difficoltŕ a realizzare compiti facili
Sbagliare nel gestire il conto in banca o difficoltŕ in fare una firma. Non riesce a fare una telefonata
9. Improvvisi cambiamenti di umore
Si arrabbiano, diventano lunatici e alcune volte anche violenti… senza motivazione
10. Difficoltŕ nell’uso di oggetti molto familiari.
Sbagliare ad usare le posate quando si mangia. Sapere cosa č un pettine, ma non ricordarsi come si usa.
Commenti dell’Associazione Alzheimer – Asti
-
Non tutti i sintomi si presentano allo stesso tempo.
-
Una perdita di memoria non vuol dire che sia l’inizio del morbo di Alzheimer.
-
I cambiamenti di personalitŕ e soprattutto il calo d’interesse per le attivitŕ sono comuni quando si arriva ad una certa etŕ.


Immagine istopatologica di placche senili nella corteccia cerebrale di una persona affetta da Morbo di Alzheimer.
La malattia č dovuta a una diffusa distruzione di neuroni, principalmente attribuita alla betamiloide, una proteina che, depositandosi tra i neuroni, agisce come una sorta di collante, inglobando placche e grovigli "neurofibrillari". La malattia č accompagnata da una forte diminuzione di acetilcolina nel cervello (si tratta di un neurotrasmettitore, ovvero di una molecola fondamentale per la comunicazione tra neuroni, e dunque per la memoria e ogni altra facoltŕ intellettiva). La conseguenza di queste modificazioni cerebrali č l'impossibilitŕ per il neurone di trasmettere gli impulsi nervosi, e quindi la morte dello stesso, con conseguente atrofia progressiva del cervello nel suo complesso.
A livello neurologico macroscopico, la malattia č caratterizzata da una diminuzione nel peso e nel volume del cervello, dovuta ad atrofia corticale, visibile anche in un allargamento dei solchi e corrispondente appiattimento delle circonvoluzioni.
A livello microscopico e cellulare, sono riscontrabili depauperamento neuronale, placche senili (dette ancheplacche amiloidi), ammassi neurofibrillari, angiopatia congofila (amiloidea).
Dall'analisi post-mortem di tessuti cerebrali di pazienti affetti da Alzheimer (solo in tale momento si puň confermare la diagnosi clinica da un punto di vista anatomo-patologico), si č potuto riscontrare un accumulo extracellulare di una proteina, chiamata Beta-amiloide.
Nei soggetti sani la APP (Amyloid precursor protein, Proteina Progenitrice dell'Amiloide), attraverso una reazione biologica catalizzata dall'alfa-secretasi, produce un peptide innocuo chiamato p3. Per motivi non totalmente chiariti, nei soggetti malati l'enzima che interviene sull'APP non č l'alfa-secretasi ma una sua variante, la beta-secretasi, che porta alla produzione di un peptide di 40-42 aminoacidi: la beta-amiloide.
Tale beta-amiloide non presenta le caratteristiche biologiche della forma naturale, ma tende a depositarsi in aggregati extracellulari sulla membrana dei neuroni. Tali placche neuronali innescano un processo infiammatorio che attiva una risposta immunitaria richiamando macrofagi e neutrofili, i quali produrranno citochine, interleuchine e TNF-alfa che danneggiano irreversibilmente i neuroni.
Ulteriori studi mettono in evidenza che nei malati di Alzheimer interviene un ulteriore meccanismo patologico: all'interno dei neuroni una Proteina Tau, fosforilata in maniera anomala, si accumula nei cosiddetti "aggregati neurofibrillari" (o ammassi neurofibrillari).
Particolarmente colpiti da questo processo patologico sono i neuroni colinergici, specialmente quelli delle aree corticali, sottocorticali e, tra queste ultime, le aree ippocampali.
In particolare, l'ippocampo č una struttura encefalica che svolge un ruolo fondamentale nell'apprendimento e nei processi di memorizzazione; perciň la distruzione dei neuroni di queste zone č ritenuta essere la causa principale della perdita di memoria dei malati.


Compiere attivitŕ intellettive, come giocare a scacchi o mantenere regolari rapporti sociali, č considerato un modo per prevenire la malattia di Alzheimer.
Al momento non ci sono prove definitive per sostenere l'efficacia di una qualsiasi misura preventiva per la malattia di Alzheimer. Studi per identificarle hanno spesso prodotto risultati inconsistenti. Tuttavia, studi epidemiologici hanno proposto le relazioni tra alcuni fattori modificabili, come la dieta, il rischio cardiovascolare, l'utilizzo di prodotti farmaceutici, o lo svolgimento di attivitŕ intellettuali e la probabilitŕ di una popolazione di sviluppare il la malattia. Solo ulteriori ricerche, tra cui gli studi clinici, riveleranno se questi fattori possono aiutare a prevenire o ritardale l'insorgenza del morbo di Alzheimer.
Sebbene i fattori di rischio cardiovascolari, come l'ipercolesterolemia, l'ipertensione, il diabete e il fumo, sono associati con un rischio maggiore di insorgenza della malattia, le statine, che sono farmaci per l'abbassamento del colesterolo, non si sono verificate efficaci nel prevenire o migliorare il decorso. I componenti di una dieta mediterranea, che comprendono frutta e verdura, pane, grano e altri cereali, olio d'oliva, pesce e vino rosso, possono singolarmente o tutti insieme ridurre il rischio e ritardare il decorso della malattia di Alzheimer. I loro benefici effetti cardiovascolari sono stati proposti come il meccanismo di azione. Ci sono prove limitate che un consumo, da lieve a moderato, di alcool, soprattutto vino rosso, sia associato a un minor rischio di Alzheimer.
Ipotesi sull'uso di vitamine non hanno trovato prove sufficienti di efficacia per raccomandare la vitamina C, E o acido folico, con o senza vitamina B12, come agenti di prevenzione o per il trattamento dell'Alzheimer. Inoltre, la vitamina E, č associata a rischi per la salute. Studi compiuti esaminando la somministrazione di acido folico (B9) e di altre vitamine B non hanno mostrato alcuna correlazione significativa con il declino cognitivo.
L'utilizzo a lungo termine di farmaci anti-infiammatori non steroidei (FANS) č associato ad una ridotta probabilitŕ di sviluppare Alzheimer. Studi post-mortem umani, in modelli animali, o in studi in vitro supportano il l'ipotesi che i FANS possano ridurre l'infiammazione correlata alle placche amiloidi. Tuttavia, studi riguardanti il loro uso come trattamento palliativo non sono riusciti a dimostrare risultati positivi, mentre nessun processo di prevenzione č stato realizzato. La curcumina del curry ha mostrato una certa efficacia nel prevenire i danni cerebrali, nei modelli di topo, in virtů delle sue proprietŕ anti-infiammatorie. La terapia ormonale sostitutiva, anche se utilizzata in precedenza, non č piů ritenuta efficace per prevenire la demenza e in alcuni casi puň anche essere ritenuta responsabile.
Le persone che si impegnano in attivitŕ intellettuali, come la lettura, i giochi da tavolo, i cruciverba, suonare strumenti musicali o che hanno una regolare interazione sociale, mostrano una riduzione del rischio di sviluppo della malattia di Alzheimer. Questo č compatibile con la teoria della riserva cognitiva, in cui si afferma che alcune esperienze di vita forniscono all'individuo una riserva cognitiva che ritarda l'insorgenza di manifestazioni di demenza. L'apprendimento di una seconda lingua, anche in tarda etŕ, sembra ritardare la malattia di Alzheimer. L'attivitŕ fisica č anche associata ad un ridotto rischio di Alzheimer.
Alcuni studi hanno mostrato un aumentato rischio di sviluppare la malattia nel caso di assunzione di metalli ed in particolare alluminio, o se espositi a particolari solventi. La qualitŕ di alcuni di questi studi č stata perň criticata, e altri studi hanno concluso che non vi č alcuna relazione tra questi fattori ambientali e lo sviluppo di Alzheimer.
Mentre alcuni studi suggeriscono che l'esposizione a campi elettromagnetici a bassa frequenza puň aumentare il rischio di sviluppare la malattia di Alzheimer, i revisori hanno rilevato che ulteriori indagini epidemiologiche e di laboratorio sono necessari prima di avvalorare questa ipotesi. Il fumo č un importante fattore di rischio per l'Alzheimer.
Alcun studi (National Institute on Ageing di Baltimora) ipotizzano come il digiuno ad intervalli regolari (1 o 2 giorni a settimana) possa risultare come un palliativo alle forme piů gravi della malattia.

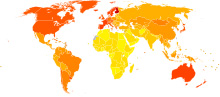
Disabilitŕ per Alzheimer e altre forme di demenza per 100.000 abitanti nel 2004.
|
nessun dato |
|
|
≤ 50 |
|
|
50–70 |
|
|
70–90 |
|
|
90–110 |
|
|
110–130 |
|
|
130–150 |
|
|
150–170 |
|
|
170–190 |
|
|
190–210 |
|
|
210–230 |
|
|
230–250 |
|
|
≥ 250 |
Le fasi iniziali della malattia di Alzheimer sono difficili da diagnosticare. Una diagnosi definitiva č posta solitamente una volta che si verifica una significativa compromissione cognitiva e una percepibile riduzione di capacitŕ di svolgere le attivitŕ della vita quotidiana, anche se la persona č ancora in grado di gestirsi autonomamente. Il deterioramento della memoria e il peggioramento dei disturbi cognitivi e non cognitivi, associati alla malattia, riducono progressivamente l'autonomia nella vita quotidiana.

I problemi di memoria sono uno dei primi segni del morbo di Alzheimer.
Alcune persone che hanno problemi di memoria in realtŕ sono affette da un altro tipo di disturbo, una compromissione cognitiva amnesica lieve (MCI amnesica), hanno piů problemi di memoria rispetto alle persone sane della loro etŕ, ma i loro sintomi non sono cosě gravi come quelli del morbo di Alzheimer. Le persone affette da MCI hanno tuttavia maggiori probabilitŕ di sviluppare il morbo di Alzheimer rispetto a quelle sane.
Anche altri cambiamenti possono essere segnali d’allarme dei primissimi stadi del morbo di Alzheimer: esisterebbe per esempio una connessione tra alcune difficoltŕ di movimento e la MCI amnesica e sono state evidenziate connessioni tra alcuni problemi di olfatto ed i problemi cognitivi.
Sintomi Alzheimer lieve
Con il progredire della malattia continua la perdita di memoria e appaiono alterazioni in altre abilitŕ cognitive, tra i problemi frequenti possiamo individuare la tendenza a:
-
perdere l’orientamento,
-
aver problemi quando si maneggia il denaro o si deve pagare il conto,
-
ripetere le domande,
-
impiegare piů tempo del solito a svolgere le normali attivitŕ,
-
non valutare correttamente le situazioni,
-
cambiare l’umore e la personalitŕ.
La prima diagnosi di solito avviene in questa fase.
I principali sintomi caratteristici di questo stadio sono:
-
Il malato sembra non aver piů voglia né gusto di vivere: non intraprende alcuna attivitŕ.
-
Perde la memoria dei fatti recenti, perň questo non si nota né dall’aspetto fisico né dalla conversazione casuale.
-
Perde confidenza con i soldi.
-
Ha difficoltŕ nell’imparare cose nuove e nel fissarle nella memoria.
-
Ha problemi a trovare le parole: puň sostituire o inventare parole che assomigliano a quelle dimenticate, o hanno un significato simile.
-
Puň smettere di parlare per evitare di commettere errori.
-
La capacitŕ di concentrazione diminuisce, cosě come la motivazione a continuare l’attivitŕ che sta svolgendo.
-
Si perde con facilitŕ, anche nei luoghi che gli sono familiari.
-
Oppone resistenza al cambiamento o alle novitŕ.
-
Ha problemi a organizzarsi e a pensare in modo logico.
-
Ripete le stesse domande piů volte.
-
Si ritira in sé stesso, perde interesse, č irritabile; non č piů sensibile ai sentimenti degli altri; č insolitamente arrabbiato in situazioni di stanchezza o di frustrazione.
-
Non prende decisioni, ad esempio quando gli si chiede cosa vuol mangiare afferma: “Prendo quel che prendi tu.”
-
Impiega piů tempo del solito per fare i lavori di casa ed č turbato se deve fare in fretta o se avviene qualcosa di imprevisto.
-
Dimentica di pagare, paga di piů del dovuto o dimentica come si fa per pagare: puň dare al cassiere il portafoglio, anziché la somma di denaro richiesta.
-
Dimentica di mangiare, mangia solo un certo alimento oppure mangia in continuazione.
-
Perde le cose o le mette al posto sbagliato; le nasconde in luoghi insoliti o dimentica dove andrebbero sistemate, ad esempio mettendo i vestiti in lavastoviglie.
-
Controlla, cerca o ammucchia costantemente cose senza alcun valore.
Sintomi Alzheimer moderato
In questo stadio i danni si verificano nelle zone del cervello che controllano
-
il linguaggio,
-
il ragionamento,
-
l’elaborazione delle informazioni sensoriali,
-
il pensiero cosciente.
La perdita di memoria e la confusione aumentano e i malati iniziano ad avere problemi nel riconoscere i famigliari e gli amici. Possono non essere in grado di imparare cose nuove, di svolgere dei compiti che comportano una successione di passaggi (ad esempio vestirsi) o di affrontare situazioni nuove. Possono avere allucinazioni, manie e paranoie, e possono comportarsi impulsivamente.
In questo stadio i cambiamenti che č possibile riconoscere sono:
-
Le alterazioni del comportamento, le preoccupazioni per l’aspetto fisico, per l’igiene e per il sonno diventano piů frequenti.
-
Confonde le identitŕ delle persone: puň pensare che suo figlio sia in realtŕ suo fratello o che la moglie sia un’estranea.
-
I problemi intellettivi causano minacce alla sua sicurezza, se lo si lascia solo: puň vagabondare e non rendersi conto dei rischi che corre, puň avvelenarsi, cadere, trascurarsi o farsi raggirare da qualche malintenzionato.
-
Ha dei problemi a riconoscere le persone che gli sono familiari e gli oggetti che gli appartengono; puň appropriarsi di cose non sue.
-
Ripete in continuazione storie, parole o frasi che gli piacciono oppure movimenti, come ad esempio strappare fazzoletti di carta.
-
Nel tardo pomeriggio o alla sera compie movimenti ripetitivi, senza sosta: ad esempio puň camminare, girare i pomelli delle porte o toccare le tende.
-
Non č in grado di organizzare i pensieri né di seguire spiegazioni logiche.
-
Ha dei problemi a seguire appunti scritti o a portare a termine delle attivitŕ.
-
Si inventa delle bugie per riempire i buchi di memoria. Ad esempio, potrebbe dire: “Tanto arriverŕ mia madre, quando avrŕ finito di lavorare”.
-
Puň essere in grado di leggere, ma non di formulare la risposta corretta a una domanda scritta.
-
Puň accusare, minacciare, imprecare, agitarsi o comportarsi in modo inadeguato, ad esempio dando calci e pugni, mordendo, gridando o graffiando.
-
Puň trascurarsi o dimenticare le buone maniere.
-
Puň avere allucinazioni visive, uditive o sensoriali.
-
Puň accusare il coniuge di avere un’altra relazione o i famigliari di avergli rubato qualcosa.
-
Si appisola con frequenza oppure si sveglia in piena notte credendo che sia l’ora di andare al lavoro.
-
Ha maggiori difficoltŕ a posizionare il proprio corpo quando usa il water o si siede.
-
Puň pensare che l’immagine dello specchio lo segua o che le vicende trasmesse in tv accadano a lui/lei.
-
Ha bisogno di aiuto per trovare il bagno, per usare la doccia, per ricordarsi di bere e per vestirsi in maniera adatta al tempo o alla circostanza.
-
La sua condotta sessuale č inappropriata: puň scambiare il coniuge per qualcun altro. Dimentica quali sono i comportamenti privati, e puň svestirsi o masturbarsi in pubblico.
Alzheimer grave
Arrivati all’ultimo stadio le placche e gli ammassi si sono diffusi in tutto il cervello ed il tessuto cerebrale ha diminuito di molto le sue dimensioni. Le persone affette da Alzheimer grave non riescono a comunicare e sono completamente dipendenti da chi si prende cura di loro. Quando l’organismo č vicino alla fine il paziente puň dover restare nel letto per la maggior parte del tempo o sempre.
In questa fase i cambiamenti riconoscibili possono essere:
-
Non riconosce se stesso né i parenti.
-
Pronuncia parole senza senso, č muto o si fa capire con difficoltŕ.
-
Puň rifiutarsi di mangiare, puň soffocare o dimenticarsi di deglutire.
-
Puň urlare in continuazione oppure toccare tutto quel che vede.
-
Perde il controllo dell’intestino e della vescica.
-
Dimagrisce e quindi la pelle diventa sottile e si ferisce facilmente.
-
Puň essere a disagio o urlare quando lo si sposta o tocca.
-
Dimentica come si fa a camminare, oppure non č abbastanza sicuro da stare in piedi o camminare da solo.
-
Puň soffrire di convulsioni; spesso puň cadere e farsi male, oppure soffrire di infezioni.
-
Puň lamentarsi, urlare o borbottare ad alta voce.
-
Dorme di piů.
-
Ha bisogno di assistenza per tutte le attivitŕ quotidiane.
Ultime notizie
|
29/03/2025 VIARIGI: prende avvio il progetto "CAFFČ ALZHEIMER E NON SOLO...per il territorio di Asti-Nord" Sotto l'egida del Consorzio COGESA e la collaborazione di Alzheimer Asti OdV, dell'ASL-AT e del Comune di Viarigi venerdì 21 marzo, inizio di primavera, ha mosso i primi passi il progetto che è... |
|
21/02/2025 Avv. Roviello et al.: "Scelte per la tutela dei nostri anziani in difficoltŕ Presso la sede serata con molti consulenti tutti preparati e disponibili. L'Avv. Donatella Roviello ha iniziato parlando dell'Amministrazione di Sostegno, le procedure e le modalità per richiederlo.... |
|
07/02/2025 In questa serata le due esperte, Erika Stefanelli e Monica Brosio, che hanno predisposto il proprio intervento con l'aiuto di paola Rabino, che è la decana dei nostri collaboratori, hanno spiegato quali... |
|
24/01/2025 dr.ssa Morando: La nutrizione nelle varie fasi della demenza La persona affetta da demenza ha un alto rischio di malnutrizione. La dr.ssa Morando ha anche illustrato le linee guida per la nutrizione nelle fasi avanzate e terminali della malattia. |
|
19/01/2025 Lancet: sono 14 le azioni che riducono il rischio di demenza nel corso della vita Ai primi di agosto è uscito l'aggiornamento del report della Lancet Commission on Dementia: Lancet è la prestigiosa rivista medica dell'Università di Oxford. Queste sono le 14 azioni: 1)... |